Se denomina síndrome metabólico (también conocido como síndrome X, síndrome plurimetabólico, síndrome de insulinorresistencia, síndrome de Reaven o CHAOS en Australia) a la conjunción de varias enfermedades o factores de riesgo en un mismo individuo que aumentan su probabilidad de padecer una enfermedad cardiovascular o diabetes mellitus.1 2 En los Estados Unidos, de acuerdo con las definición de Síndrome metabólico hecha por la NCEP (siglas del inglés: National Cholesterol Education Program-Adult Treatment Panel III), alrededor del 25% de la población mayor de 20 años padece del síndrome metabólico,3 el punto donde el individuo tiene la concomitante característica de obesidad central (localizada en el abdomen) y una resistencia a la insulina.
Respecto de los perfiles de la edad de los candidatos a padecer de Síndrome Metabólico, éste ha ido bajando de forma dramática. Si antes se hablaba de pacientes que bordeaban los 50 años, ahora el grupo de riesgo está situado en torno a los 35 años, ello porque desde etapas muy tempranas de la vida, las personas adoptan malos hábitos de alimentación y escaso ejercicio físico.
Las primeras descripciones de la asociación existente entre diversas situaciones clínicas como la diabetes mellitus (DM), la hipertensión arterial (HTA) y la dislipidemia (DLP) datan de la década de los 20 del pasado siglo, aunque el término "síndrome metabólico" se usaba a finales de los 70 para designar solo a factores de riesgos asociados con diabetes.4 5 Un hallazgo interesante por Marsella Jean Vague, en 1947 y luego en 1956, demostró que las personas con obesidad estaban predispuestos a tener en el futuro diabetes, aterosclerosis, agrandamiento de la tiroides y cálculos urinarios.6 7
Para la segunda mitad de los años 1960, Avogaro y Crepaldi describieron a seis pacientes con signos moderados de obesidad, colesterol alto y una marcada hipertrigliceridemia y estos signos mejoraron con una dieta baja en calorías y baja en carbohidratos.8 En 1977, Haller empleó el término «síndrome metabólico» para referirse a una asociación entre obesidad, diabetes mellitus e hígado graso, describiendo además los factores de riesgo de la arteriosclerosis.9 El mismo término fue usado por Singer ese año para referirse a una combinación de síntomas tales como la obesidad, bocio, diabetes mellitus y la hipertensión arterial.10 En 1977-78 Gerald B. Phillips argumentó que los factores de riesgo subyacentes a un infarto de miocardio contribuyen a formar una constelación de anomalías no sólo asociados con enfermedades del corazón, sino también con la obesidad y otros factores clínicos, y que su identificación podría prevenir enfermedades cardiovasculares.11 12
Síndrome X
Sin embargo, fue Gerald Reaven quien sugirió en su conferencia de Banting, en 1988, que estos factores tendían a ocurrir en un mismo individuo en la forma de un síndrome que denominó «X» en el que la resistencia a la insulina constituía el mecanismo fisiopatológico básico,13 proponiendo 5 consecuencias de ésta, todas ellas relacionadas con un mayor riesgo de enfermedad coronaria, cardiopatía isquémica, disfunción ventricular izquierda y fallo cardiaco. Los componentes originales del Síndrome X de Reaven eran:14
Resistencia a la captación de glucosa mediada por insulina
Intolerancia a la glucosa
Hiperinsulinemia
Aumento de triglicéridos en las VLDL
Disminución del colesterol tipo HDL
Hipertensión arterial
A lo largo de los años se ha ido añadiendo más componentes a la definición de este síndrome, a la vez que comenzó a recibir nuevas denominaciones como Síndrome X plus, Cuarteto mortífero, Síndrome plurimetabólico, Síndrome de insulinorresistencia, entre otros.15 En 1998, un grupo consultor de la OMS propuso que se denominara Síndrome metabólico (SM) y sugirió una definición de trabajo que sería la primera definición unificada del mismo.16
Epidemiología
La prevalencia del síndrome metabólico varía en dependencia de la definición empleada para determinarla, así como de la edad, el sexo, el origen étnico y el estilo de vida. Cuando se emplean criterios parecidos a los de la OMS, la prevalencia del SM varía del 1,6 al 15 % en dependencia de la población estudiada y del rango de edad.17 El estimado de prevalencia en EE.UU. es del 22 %, varía del 6,7 % en las edades de 20 a 43,5 años a 43,5 % en los mayores de 60 años, no se han reportado diferencias por sexo (23,4 % en mujeres y 24 % en hombres).18
La prevalencia de SM en Chile es equivalente a la de Estados Unidos de Norteamérica.14 Entre 1986 y 1998 la obesidad en Chile aumentó de 4,6% a 24,0% en los prepúberes y de 2,3% a 17% en adolescentes,14 mientras que la prevalencia del síndrome metabólico en adultos es de 22,6%; 23% en hombres y 22,3% en mujeres.14 En poblaciones de alto riesgo, como la de familiares de personas con diabetes, la prevalencia aumenta a casi 50%, llegando a más de 80% en personas diabéticas.19
En Europa, la prevalencia del síndrome metabólico en niños es variable, desde un 33% en el Reino Unido hasta un 27 y 9% en Turquía y Hungría, respectivamente. En España, por su parte, un estudio demostró que la prevalencia es de un 17-18% en la población pediátrica con obesidad moderada.20
En poblaciones de alto riesgo, como la de familiares de personas con diabetes, la prevalencia aumenta considerablemente hasta casi el 50 %, llega a más del 80 % en personas diabéticas y al 40 % en personas con intolerancia a la glucosa.21
Etiología
La causa del síndrome metabólico se desconoce. Su fisiopatología es extremadamente compleja y solo ha sido dilucidada una parte de ella. La mayoría de los pacientes tienen una edad considerablemente mayor, son obesos, sedentarios, y tienen cierto grado de resistencia a la insulina. La resistencia a la insulina juega un papel central en la génesis de este síndrome. La hiperinsulinemia, es decir, una concentración elevada de insulina en el plasma sanguíneo, resulta ser un factor de riesgo independiente para la aparición de enfermedad isquémica del corazón, ayuda a la aparición temprana de la diabetes y a su progresión susecuente, y contribuye a la aparición de otro número de patologías asociadas que se traducen en factores de riesgo cardiovascular.22
La resistencia a la insulina se define como una condición en la cual las cantidades de insulina producidas fisiológicamente producen una respuesta biológica reducida, es decir, una reducción de la capacidad de acción de la insulina en el control metabólico de la glucosa después de una comida, se asocia con supresión inadecuada de insulina en ayunas la noche, en presencia de una producción conservada de la hormona. Tras la resistencia a la insulina aparece una hiperinsulinemia compensadora, demostrado con el hallazgo de elevadas concentraciones de insulina en ayunas y después de las comidas.
Actualmente la insulinorresistencia se considera como la responsable de la mayor parte de las anomalías presentes en este padecimiento, fundamentalmente de la hiperglucemia, la hipertensión arterial, el aumento en la producción hepática de VLDL y triglicéridos y la estimulación de la proliferación endotelial por acción sobre receptores endoteliales causante del inicio del proceso de aterosclerosis.23 Los mecanismos moleculares causantes de la insulinorresistencia y el SM no están claros, entre estos se proponen:
Mal nutrición fetal y bajo peso al nacer24
Incremento en la adiposidad visceral, tan solo la obesidad entre el arco costal y la cintura es indicativo de resistencia a la insulina
Anomalías genéticas de una o más proteínas en la cascada de acción de la insulina
Niveles reducidos de receptores de la insulina
Actividad tirosincinasa en músculo esquelético (no parece defecto primario)
Defectos posreceptores
Defecto en la señalización PI - 3 kinasa que causa reducción de traslocación de GLUT - 4 a la membrana plasmática (foco actual en la patogénesis)25
Un gran número de marcadores del sistema de inflamación, incluyendo la Proteína C reactiva, se incrementan durante esta enfermedad, como lo son el fibrinógeno, la interleucina 6 (IL-6), el Factor de Necrosis Tumoral-alfa (TNFα) y otros. Algunos otros señalan que es debido al estrés oxidativo, que tiene una gran variedad de causas entre ellas el incremento de los niveles de ácido úrico causado por las dietas con niveles altos de fructosa.26 27 28 Estas moléculas pro-inflamatorias producen, lipolisis, angiogénesis, disfunción endotelial, vasoconstricción, fibrinólisis y resistencia a la insulina.
La leptina, una hormona descubierta recientemente, regulada por el gen ob, que aunque no está incluida directamente en los ejes metabólicos anteriores, parece ser un componente de disfunción hormonal en el SM como marcador importante de la cantidad de tejido adiposo en el cuerpo. Aunque se produce principalmente por el adipocito, su función principal es la regulación del nivel de saciedad a nivel hipotalámico, y juega un papel importante en la reproducción humana. Algunos de los efectos de la leptina in vitro son la atenuación de la acción de la insulina en los hepatocitos, el aumento de la oxidación de ácidos grasos, la disminución de triglicéridos en los adipocitos y disminución de la unión de la insulina a los adipocitos. Así, la leptina es uno de los responsables de la modulación de la acción y la sensibilidad a la insulina. Por otra parte, su asociación con el eje gonadal y, posiblemente, con los ejes y corticotropico/
Diagnóstico
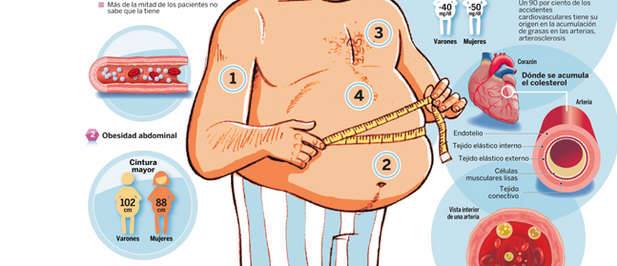
Uno de los criterios para diagnosticar el SM en adultos es la obesidad abdominal.30
En la actualidad hay dos grandes definiciones de síndrome metabólico proporcionados por la Federación Internacional de Diabetes (IDF por sus siglas en inglés)31 y la revisión del National Cholesterol Education Program,32 respectivamente, aunque ambas son muy similares. Las dos diferencias, la primera es que la IDF excluye cualquier individuo sin un incremento del diámetro de la cintura, mientras que en la definición de la NCEP el padecimiento puede ser diagnosticado con base a otros criterios; y la segunda es el uso de puntos en específico para la medición del diámetro de la cintura por parte de la IDF, mientras que la NCEP no utiliza puntos en específico.
La microalbuminuria, como marcador de disfunción endotelial, daño vascular, daño renal y enfermedad cardiovascular, es un criterio clínico para la definición de síndrome metabólico según la OMS.33
OMS
Los criterios de la Organización Mundial de la Salud (1999) requieren la presencia de diabetes mellitus, tolerancia anormal a la glucosa, glucemia de ayuno anormal o resistencia a la insulina, MÁS dos de los siguientes:32
Presión arterial ≥ 140/90 mmHg
Dislipidemia: triglicéridos (TG): ≥ 1.695 mmol/L y/o colesterol HDL (HDL-C) ≤ 0.9 mmol/L (en hombres), ≤ 1.0 mmol/L (en mujeres)
Obesidad central: relación cintura/cadera > 0.90m (en hombres), > 0.85m (en mujeres), y/o índice de masa corporal (IMC) > 30 kg/m2
Microalbuminuria: excreción urinaria de albúmina ≥ 20 mg/min o relación albúmina/creatinina en orina ≥ 30 mg/g33
Tratamiento
Hacer ejercicio y adelgazar son medidas útiles para mejorar la sensibilidad a la insulina y reducir la presión arterial y los niveles de colesterol.36
El tratamiento sugerido es principalmente tener un estilo sano de vida, es decir, la restricción de calorías y la actividad física. Sin embargo, el tratamiento farmacológico es a menudo necesario. La reducción de peso y el incremento de la actividad física conducen a la reducción efectiva de todos los factores de riesgo cardiovasculares al mejorar la sensibilidad a la insulina y reducir el riesgo de enfermedades cardiovasculares. La reducción de peso, aun moderada (10 % del peso inicial), conduce a una disminución del LDL-C, mejora todos los factores de riesgo y disminuye el riesgo vascular global del paciente.37 Los beneficios de la disminución de la tensión arterial, disminución de los lípidos y control de la glucemia sobre la morbilidad y la mortalidad han quedado bien demostrados por ensayos clínicos controlados a largo plazo, de manera que actualmente se recomienda el tratamiento agresivo de cada una de las comorbilidades del SM mediante regímenes de terapia combinada.38 En general, las enfermedades que comprenden el síndrome metabólico se tratan por separado.
Control de la glucemia
La resistencia a la insulina se considera el defecto patológico principal en individuos con diabetes tipo 2, fundamentalmente durante las primeras etapas de la enfermedad. La metformina ha sido ampliamente utilizada en la práctica clínica como agente antidiabético que mejora significativamente la sensibilidad a la insulina con efectos favorables adicionales sobre el perfil lipídico al reducir modestamente los niveles de colesterol y triglicéridos (triglicéridos en 24 %, colesterol-LDL en 10 %), se recomienda como fármaco de primera elección en diabéticos con un índice de masa corporal mayor del 27 %.39 40 41
Las glitazonas o tiazolinendionas, nueva clase de drogas antidiabéticas orales, mejoran el control metabólico en pacientes con DM2, además, reducen la resistencia a la insulina, no solo en diabéticos tipo 2 sino también en condiciones no -
Tratamiento de la dislipidemia [editar]
Deben iniciar con cambios terapéuticos en el estilo de vida (modificaciones en la dieta y actividad física, consumo de alcohol, proscripción del hábito de fumar) seguidos por tratamiento farmacológico, si después de 3 meses no se logran las metas deseables. El tratamiento farmacológico de la dislipidemia en el SM debe iniciarse con estatinas y, de ser necesario, combinar con fibratos y derivados del ácido nicotínico.42 43
A las estatinas y fibratos se les ha conferido propiedades antiaterosclerótica y antitrombótica. De manera general, con su uso se ha observado mejoría del perfil aterogénico, de la reactividad vascular dependiente de endotelio y de la sensibilidad hepática a la insulina; esta última al disminuir el exceso de acúmulo de lípidos en hígado y músculo.44
Control de la hipertensión arterial
La prescripción del fármaco antihipertensivo debe hacerse teniendo en cuenta las características clínicas y metabólicas del paciente y las propiedades del medicamento.45 Los inhibidores de las enzimas convertidoras de angiotensina y los antagonistas de los receptores de la angiotensina II se recomiendan como antihipertensivos de elección en los pacientes con SM al producir vasodilatación y disminuir los niveles de noradrenalina circulantes (efecto simpaticolítico), lo que origina un incremento en la sensibilidad a la insulina y disminución en los niveles de insulina circulante, además se demuestra que disminuyen los niveles de colesterol total y de triglicéridos en plasma.46 47
Varios metaanálisis recientes sugieren que pueden ofrecer una ventaja especial en la prevención de complicaciones cardiovasculares adicionales al control de la tensión arterial.48 49
Prevención
Se han propuesto diversas estrategias para prevenir la aparición del síndrome metabólico. Estos incluyen el aumento de la actividad física (como caminar 30 minutos al día),50 y una vida sana, dieta reducida en calorías.51 Hay muchos estudios que apoyan un estilo de vida saludable. Así lo demostró un estudio realizado con 351 pacientes de diversos orígenes.52
En el 2007, un estudio de 2,375 hombres con más de 20 años sugiere que la ingesta diaria de leche o productos lácteos equivalentes pueden reducir a la mitad el riesgo de síndrome metabólico.53 Otros estudios, tanto de apoyo y de la solución de los autores de los resultados.